Author: Dylan Daniel, PhD, Director, Scientific Development
Date: December 2016
Le cancer du sein est la deuxième malignité la plus mortelle après le cancer du poumon chez les femmes aux États-Unis, avec 246 000 nouveaux cas estimés et 40 450 décès attendus en 2016. Il existe de nombreux traitements pour le cancer du sein, comme la chirurgie, la radiothérapie, la thérapie anti-œstrogène, les thérapies ciblées (par exemple, le trastuzumab) et la chimiothérapie. Malgré ces avancées thérapeutiques, les métastases restent à l'origine d'une mortalité importante. L'immunothérapie a connu des progrès remarquables au cours des cinq dernières années, avec l'approbation de quatre inhibiteurs des points de contrôle immunitaires des lymphocytes T. Bien qu'aucun de ces inhibiteurs de point de contrôle ne soit approuvé pour le cancer du sein, il existe actuellement plus de 60 essais cliniques en cours portant sur le cancer du sein avec des inhibiteurs de point de contrôle contre les PD-1 ou PD-L1 et plus de 20 essais cliniques en cours avec des inhibiteurs CTLA-4.
Comme les inhibiteurs de points de contrôle et d'autres classes d'immunothérapies nécessitent un système immunitaire intact pour susciter une activité, les modèles murins syngéniques de cancer du sein constituent une option importante pour les essais précliniques de nouveaux agents. Labcorp has fully characterized the 4T1-luc2 mammary carcinoma model derived from Balb/c mice as an orthotopic model to support studies with novel immuno-oncology agents. Les tumeurs orthotopiques 4T1-luc2 se métastasent dans les ganglions lymphatiques et les poumons, ce qui en fait un modèle précieux pour étudier l'effet des thérapies sur les tumeurs primaires et les maladies métastatiques en utilisant l'imagerie par bioluminescence. La croissance des tumeurs 4T1-luc2 est équivalente dans les souches immunodéficientes et les souris Balb/c immuno-compétentes, ce qui suggère que 4T1-luc2 est une tumeur faiblement immunogène (figure 1).
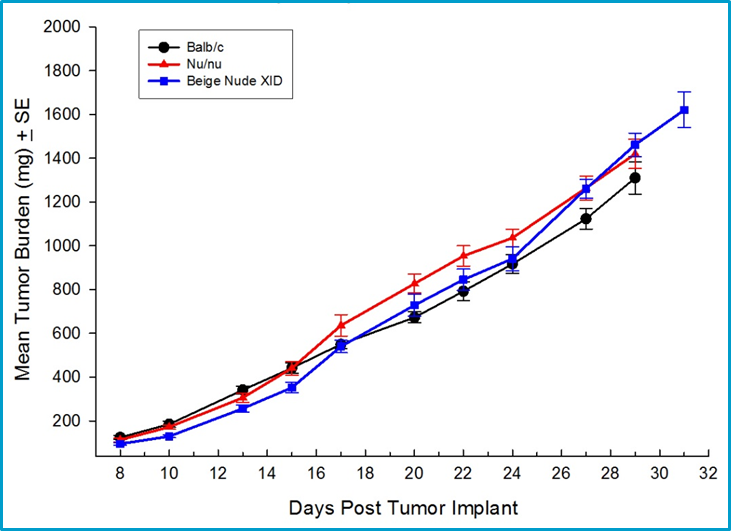
Fig. 1 : croissance orthotopique de 4T1-luc2 dans plusieurs souches de souris, y compris des souris Balb/c syngéniques.
Les études d'efficacité avec des anticorps anti-PD-1 ou anti-PD-L1 sont entravées par une réaction d'hypersensibilité mortelle chez des souris porteuses de tumeurs 4T11. Il est possible d'administrer deux doses sans toxicité, mais un dosage continu n'est pas possible. C'est l'efficacité des anti-CTLA-4 en combinaison avec des rayons localisés qui a été évaluée à la place. Un anticorps anti-CTLA-4 de hamster a été utilisé et, contre toute attente, le contrôle de l'isotype du hamster a montré une activité significative chez certaines souris (figure 2A), qu'il était impossible de distinguer de l'activité anti-CTLA-4 (figure 2B). Un bénéfice thérapeutique a été associé aux radiations localisées (figure 2C), mais aucune amélioration claire n'a été constatée avec la combinaison des radiations et des anti-CTLA-4 (figure 2D).
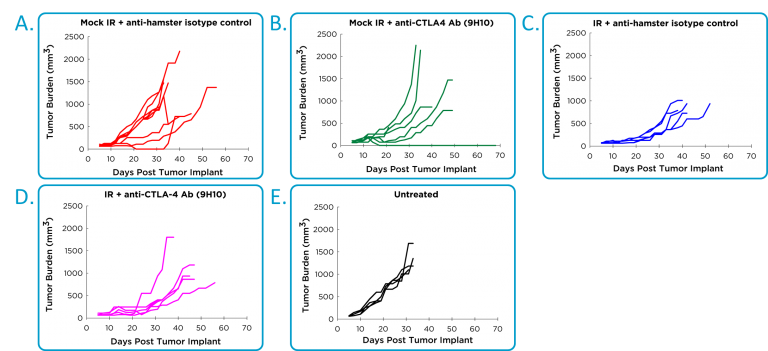
Fig. 2 : efficacité de l'anti-CTLA-4 avec radiothérapie localisée dans un modèle de tumeur mammaire 4T1-luc2 orthotopique.
La charge métastatique a été évaluée à l'aide de l'imagerie par bioluminescence, et les images présentées sont représentatives de la progression des métastases chez les souris non traitées (figure 3A). Les souris traitées aux anti-CTLA-4 avaient une charge tumorale métastatique réduite par rapport aux souris traitées aux isotypes témoins (figure 3B). Les rayons localisés ont également produit une réduction significative de la charge métastatique ; cependant, il ne semble pas y avoir d'amélioration au-delà de l'activité de l'agent unique anti-CTLA-4 dans le groupe combiné.
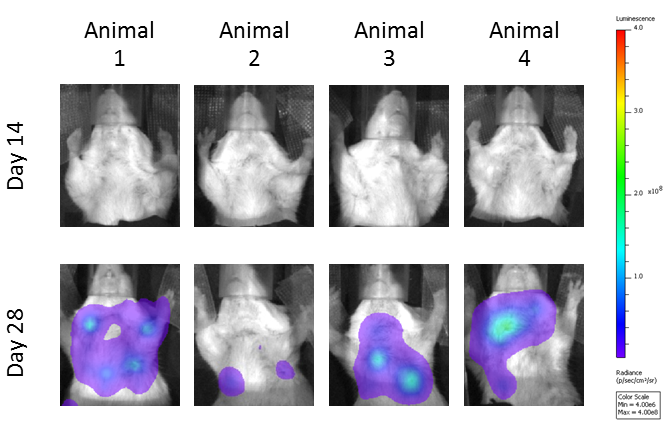
Fig. 3 : évaluation de la charge tumorale métastatique totale au cours du temps par imagerie par bioluminescence
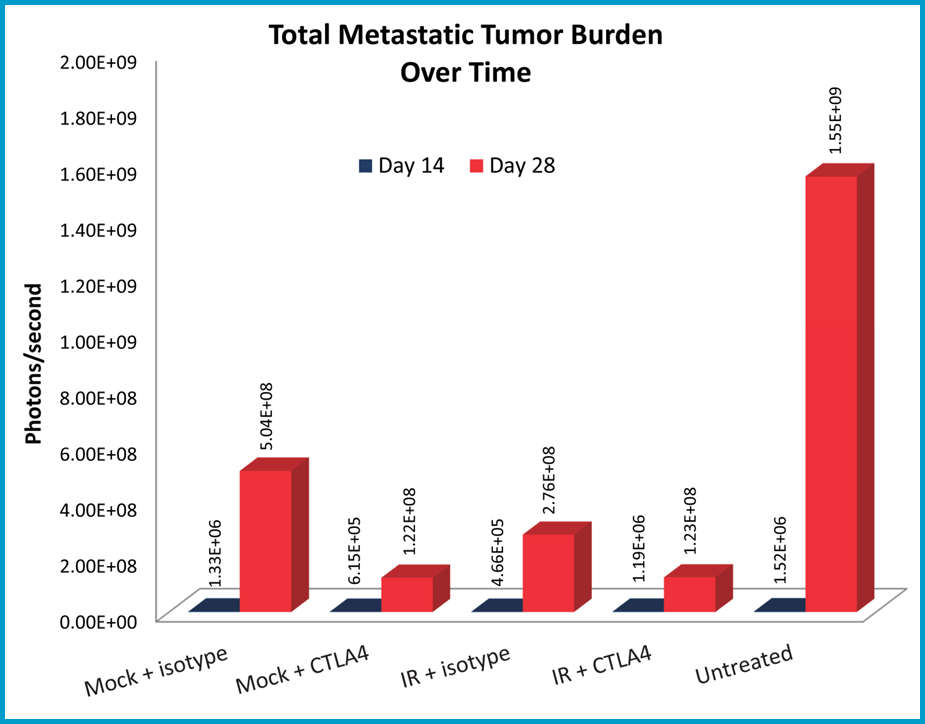
Fig 3B : quantification de la charge métastatique et réponse au traitement.
Les radiations dans cette étude ont été localisées en utilisant un blindage de plomb pour réduire l'irradiation de tout le corps ; cependant, certains animaux présentaient encore des signes de toxicité radiologique. Labcorp now offers focal beam radiation capabilities using the small animal radiation research platform (SARRP) by Xstrahl which reduces systemic radiation toxicity.
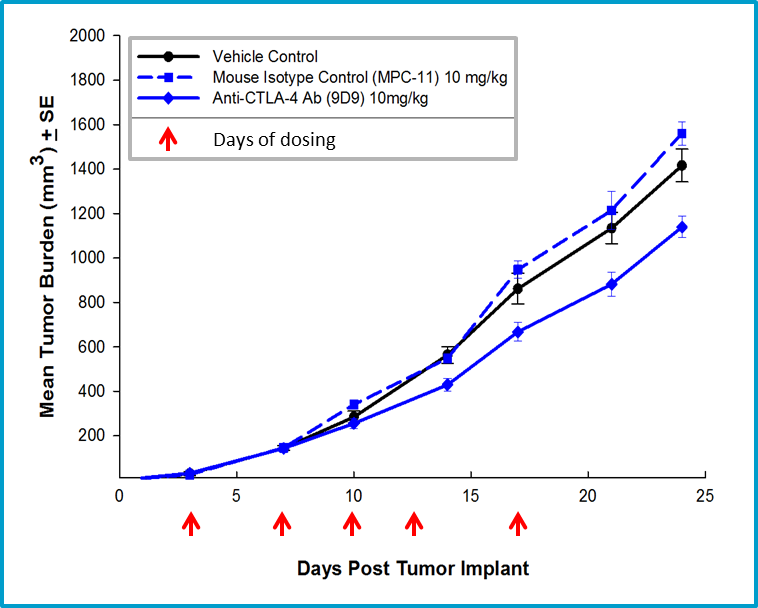
Fig. 4 : efficacité de la thérapie anti-CTLA-4 avec un anticorps anti-CTLA-4 de l'isotope de la souris.
L'activité anti-tumorale non spécifique associée à l'utilisation d'un anticorps de hamster dans le modèle 4T1-luc2 a suscité une étude ultérieure utilisant un anticorps anti-CTLA-4 de souris. Le traitement anti-CTLA-4 de la souris a entraîné une activité minimale dans le modèle 4T1-luc2 (figure 4), mais offre un partenaire potentiel pour des études de clients avec de nouveaux agents immuno-oncologiques. En outre, nous disposons d'une vaste gamme de profilage immunitaire par cytométrie en flux des tumeurs 4T1-luc2, y compris la quantification des lymphocytes T CD4, lymphocytes T CD8, les lymphocytes T régulateurs, les MDSC granulocytaires, les MDSC monocytaires, les macrophages associés aux tumeurs M1 et M2 (TAM) (figure 5). Le modèle est bien caractérisé et disponible pour des études de clients de nouvelles immunothérapies ou d'agents qui peuvent bien se combiner avec les immunothérapies disponibles dans le commerce. Please contact us for further information and find out how Labcorp can help with your next study.
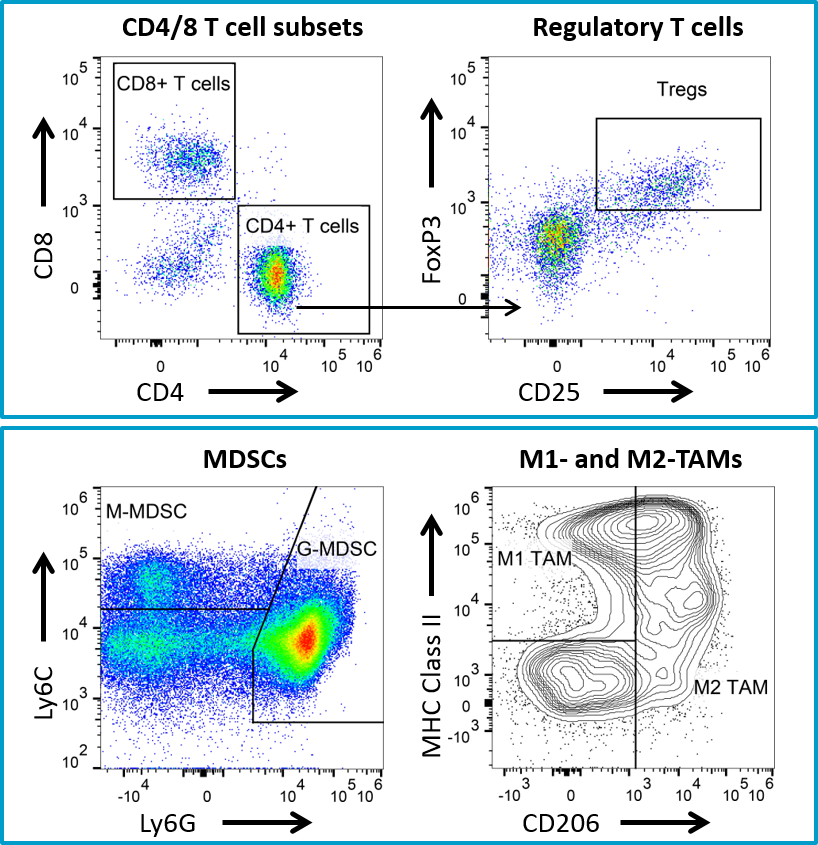
Fig. 5 : profilage immunitaire par cytométrie en flux pour les tumeurs 4T1-luc2.
1Mall et al., OncoImmunology (2016), Vol. 5 (2): e1075114
Remarques : les études ont été réalisées conformément aux réglementations applicables pour le bien-être animal et dans un centre agréé par l'AAALAC.
Références
Connexion
Entamons le dialogue
Nous contacter