Date: September 2020
L'imagerie par bioluminescence (BLI) est une modalité d'imagerie optique non invasive conçue pour visualiser et quantifier les signaux bioluminescents dans les tissus1. La BLI s'appuie sur la détection de la lumière visible produite pendant l'oxydation enzymatique d'un substrat lorsque l'enzyme est exprimée in vivo comme rapporteur moléculaire.
La BLI offre une alternative robuste, sensible et à haut débit par rapport aux études de biodistribution et à l'imagerie plus traditionnelles utilisant des critères terminaux, des procédures invasives ou le radiomarquage. We were the first CRO to offer BLI in 2003 and in the 17 years since we have amassed considerable experience and know-how in this optical imaging field. Dans cet article de notre série de présentations de technologies, nous allons vous présenter les principes de l'imagerie par bioluminescence et mettre en avant les avantages que ce service préclinique offre pour la détection des cancers, le suivi de la progression de la maladie et l'évaluation de l'efficacité antitumorale in vivo.
La BLI a besoin que les cellules expriment la luciférase, mot qui vient du latin lucifer, celui qui apporte la lumière, produite par exemple par les lucioles ou les pensées de mer. Le gène luc de la luciole a été cloné pour la première fois en 19852 et depuis, le vert est la couleur fluorescente la plus utilisée en imagerie. La luciférase des lucioles nécessite l'injection de son substrat, la D-luciférine, qui génère un signal bioluminescent culminant à 562 nm, capturé par un dispositif à transfert de charges (CCD) à haut rendement quantique placé dans une enceinte étanche à la lumière. The sequence of events leading from engineering tumor cells to express luciferase to imaging animals in vivo is illustrated in Figure 1. We use IVIS® In Vivo Imaging Systems (PerkinElmer, Waltham, MA) which allow high sensitivity and high resolution in vivo BLI and fluorescence imaging (FLI) across a wide range of wavelengths. Jusqu'à cinq animaux peuvent être soumis à l'imagerie à la fois, sous anesthésie à l'isoflurane à 2 %. Chaque souris reçoit une injection de D-luciférine et passe à l'imagerie 10 à 15 minutes après l'injection. Le signal BLI est quantifié en régions d'intérêt (ROI) dessinées autour des tumeurs, zones spécifiques (par exemple crâniennes, thoraciques ou abdominales), corps entier ou tissus ex vivo et le signal est exprimé en photons par seconde, qui représente le flux rayonnant de manière omnidirectionnelle à partir de la région définie par l'utilisateur. Les images sont analysées à l'aide du logiciel Living Image 4.3.1 (PerkinElmer, Waltham, MA).
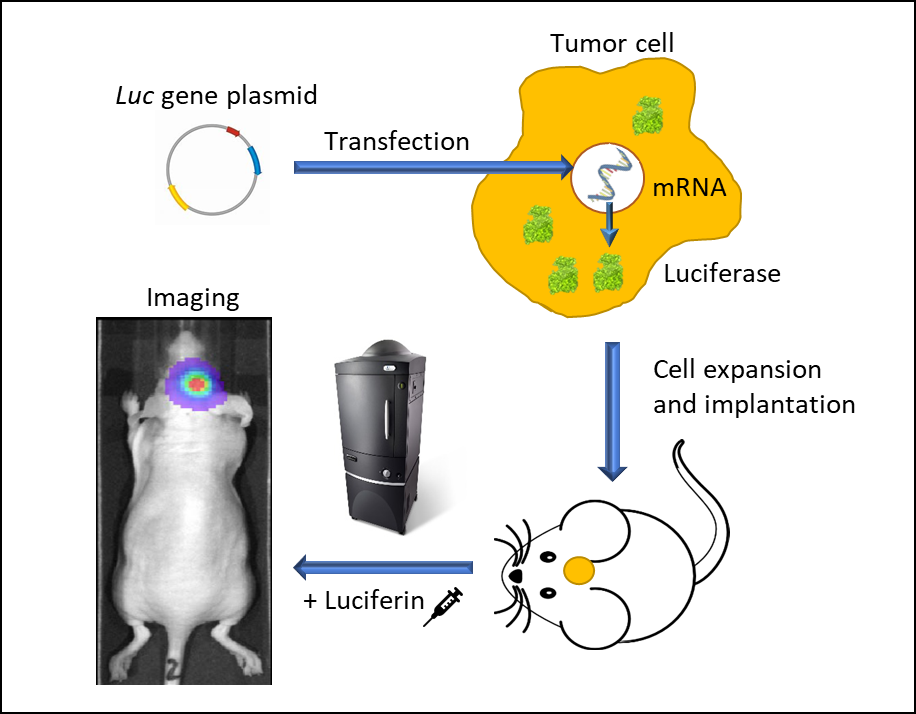
Figure 1 : imagerie par bioluminescence in vivo utilisant des cellules luminescentes vivantes. Un vecteur portant un gène luc piloté par un promoteur est transfecté dans une cellule tumorale. Les cellules transfectées de manière stable sont cultivées et implantées dans une souris. Après croissance de la tumeur, on injecte de la luciférine à l'animal et il fait l'objet d'une imagerie dans un système d'imagerie IVIS sous anesthésie. Les cellules Luc émettent de la lumière est peuvent être suivies dans l'espace et dans le temps.
Surveiller la croissance d'une tumeur solide orthotopique
Au cours des 20 dernières années, l'efficacité et la sensibilité des méthodes et outils de la BLI ont permis d'élargir sans cesse le catalogue des applications : études des interactions protéine-protéine, dépistage génétique, régulateurs du cycle cellulaire, infections parasitaires, suivi des greffes de cellules souches, migration des cellules NK et, surtout, oncologie préclinique. Plusieurs études ont montré la capacité de l'imagerie BLI à évaluer le développement des tumeurs dans le temps3. Ceci est particulièrement important lorsque la croissance de la tumeur ne peut être déterminée par des mesures au calibre et repose soit sur des signes cliniques tels que la perte de poids, soit sur l'évaluation de la charge tumorale après euthanasie des animaux. Dans les exemples ci-dessous, la prise en charge des animaux et l'utilisation de ceux-ci ont été effectuées conformément à la réglementation sur le bien-être des animaux dans un établissement accrédité par l'AAALAC, avec examen et approbation du protocole de l'IACUC.
La figure 2 présente des exemples mettant en évidence la valeur de la BLI non invasive dans la surveillance du développement des tumeurs dans des tissus profonds. Des xénogreffes de carcinome pulmonaire humain NCI-H460-Luc2 ont été implantées par voie orthotopique (OT) (1x105 cellules/souris) dans le poumon gauche de souris nude femelles. La BLI (figure 2, en haut à gauche) montre des tumeurs dans la cavité thoracique détectables dès 8 jours après l'implantation des cellules tumorales (non visibles sur l'image en raison de la définition du seuil au signal maximum observé le jour 28), et une augmentation de la charge tumorale au cours des 2 semaines suivantes. Les souris ont connu une perte de poids corporel moyenne de 18,3 % pendant toute la durée de l'étude, probablement liée à la maladie (données non présentées) et ont été euthanasiées 28 jours après l'implantation des cellules tumorales. La nécropsie a révélé une croissance significative de la tumeur primaire et un développement important de masses dans toute la cavité thoracique. Dans la figure 2, en bas à gauche, des souris albinos femelles C57BL/6 ont été implantées par voie intracrânienne avec des cellules de gliome murin syngénique GL261-luc2 (1x106 cellules/souris). Les tumeurs sont détectables dans le cerveau 7 jours après l'implantation. La perte de poids associée à la progression de la maladie est fréquente dans ce modèle et était détectable 11 jours après l'implantation de la tumeur alors que le moment médian du décès était d'environ 21 jours. La lignée cellulaire d'adénocarcinome du sein humain MDA-MB-231-luc-D3H2LN forme des lésions osseuses après injection intracardiaque (1x105 cellules/souris) chez des souris nude femelles. Les lésions osseuses étaient clairement visibles 21 jours après l'injection des cellules tumorales et tant le nombre de tumeurs que la charge tumorale totale ont augmenté au cours des 3 semaines suivantes (figure 2, à droite, en haut et en bas). Les souris ont connu une perte de poids maximum de 16,2 % au jour 32. La perte de poids était en grande partie liée à l'agressivité du modèle (données non présentées). La leçon à tirer de ces études est que la BLI peut être un outil puissant pour étudier divers types de tumeurs en temps réel et de manière non invasive sans devoir se fier uniquement aux signes cliniques de la maladie qui peuvent, ou non, accompagner une augmentation de la charge tumorale.
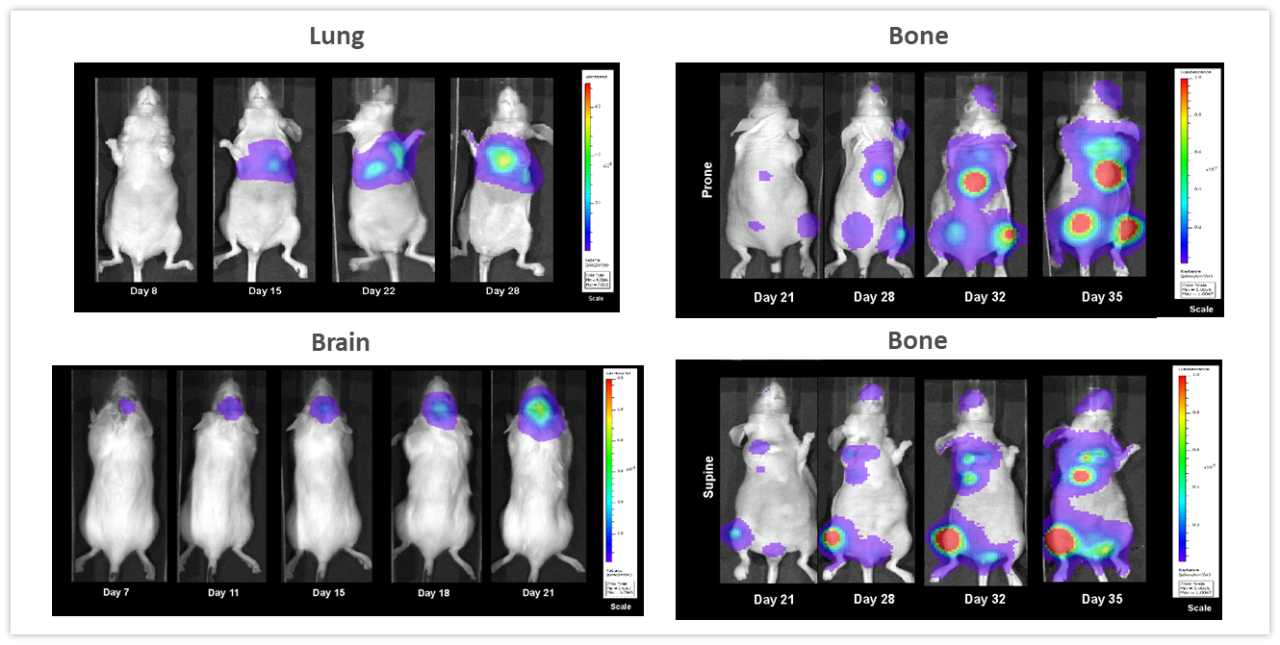
Figure 2 : Images de BLI représentatives de différents modèles in vivo. En haut à gauche, le carcinome pulmonaire humain NCI-H460-Luc2 implanté en OT (poumon gauche) chez des souris nude femelles. En bas à gauche, gliome syngénique murin GL261-luc2 implanté en OT dans le cerveau de souris albinos C57BL/6 femelles et en bas à droite, lésions osseuses de tumeur mammaire humaine MDA-MB-231-luc-D3H2LN après injection intracardiaque chez des souris nude femelles montrant des images du corps entier en position couchée sur le ventre (haut) et couchée sur le dos (bas).
L'imagerie des malignités hématologiques
With over 80 unique hematological malignancy cell lines, we lead the industry with market-relevant hematologic malignancy models, particularly pertinent in the adoptive cell therapy (ACT), also known as cellular immunotherapy, field.4 BLI is critically valuable when evaluating progression and treatment response in hematological disseminated malignancies. Des études longitudinales réalisées sur 4 différentes cellules cancéreuses hématologiques humaines injectées par voie intraveineuse à des souris NSG ont montré une augmentation de la charge tumorale au fil du temps dans tous les modèles (figure 3), ce qui montre bien la valeur de la BLI pour l'évaluation répétée de la progression et de la gravité de la maladie, ainsi que pour la compréhension de la biodistribution du signal tumoral dans tout l'organisme.
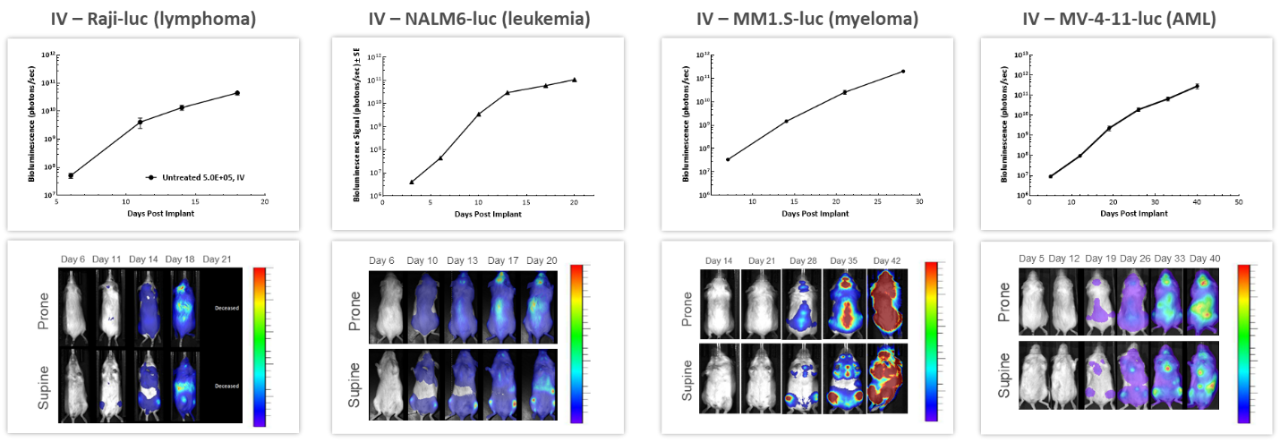
Figure 3 : données représentatives de la BLI sur plusieurs hémopathies malignes humaines in vivo après injection par voie intraveineuse chez des souris NSG.
Les ACT évoluent en permanence, fournissant de meilleures options, davantage personnalisées, aux patients. Les cellules CAR-T sont des cellules T autologues ou allogéniques qui ciblent spécifiquement des antigènes ou des marqueurs exprimés par les cellules tumorales. L'évaluation préclinique in vivo de l'efficacité et de la sécurité des cellules CAR-T est cruciale avant de transposer ces nouvelles thérapies au niveau clinique. L'étude présentée à la figure 4 a été conçue pour tester différentes préparations et doses de CAR-T dans des cellules de lymphome humain à cellules B Raji-luc implantées par voie intraveineuse chez des souris NSG. Les 3 différentes constructions à partir de cellules CAR-T ont considérablement inhibé la charge tumorale et prolongé la survie, ce qui montre la valeur que la BLI apporte au développement de ces nouvelles immunothérapies cellulaires.
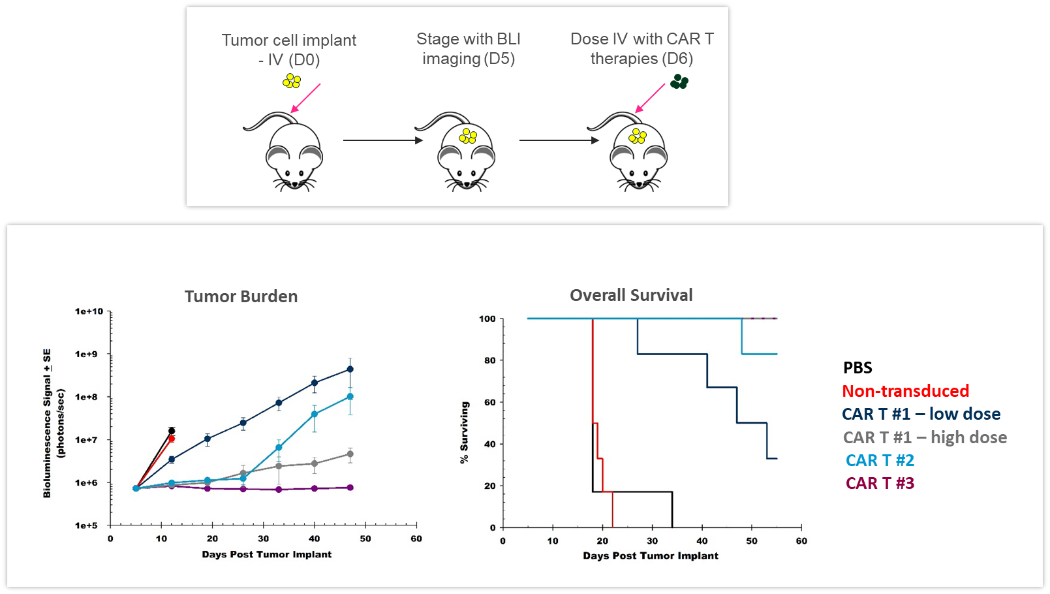
Figure 4 : effet de la thérapie CAR-T contre un lymphome humain à cellules B Raji-luc implanté par intraveineuse chez des souris NSG. En haut : diagramme schématique de l'innoculation de cellules tumorales et de la thérapie CAR-T. En bas : charge tumorale évaluée par BLI et survie globale.
Surveiller l'efficacité du traitement
Radiation
De toute évidence, l'un des principaux avantages de la BLI est la possibilité de suivre l'efficacité des thérapies antitumorales dans le temps chez un même animal, ce qui permet de réduire le nombre d'animaux utilisés. Dans l'exemple de la figure 5, des souris nude femelles se sont fait implanter par voie intracrânienne un carcinome pulmonaire non à petites cellules humain NCI-H1975-luc afin d'imiter les métastases pulmonaires dans le cerveau. Les souris ont reçu deux doses de rayons fractionnées (2 Gy ; 5 jours de traitement puis deux jours de repos sur deux cycles), délivrées par un irradiateur RadSource RS-2000. Le groupe témoin a été faussement irradié. Les images par BLI obtenues au fil du temps ont montré que les rayons réduisaient significativement la charge tumorale (figure 5, p<0,05 au jour 19) et augmentaient la durée de vie de 160 % (p<0.05, données non présentées). Dans cette expérience, nous avons pu quantifier la réponse au traitement in vivo, ce qui est critique au moment de surveiller l'efficacité et de concevoir et d'affiner de nouvelles approches thérapeutiques.
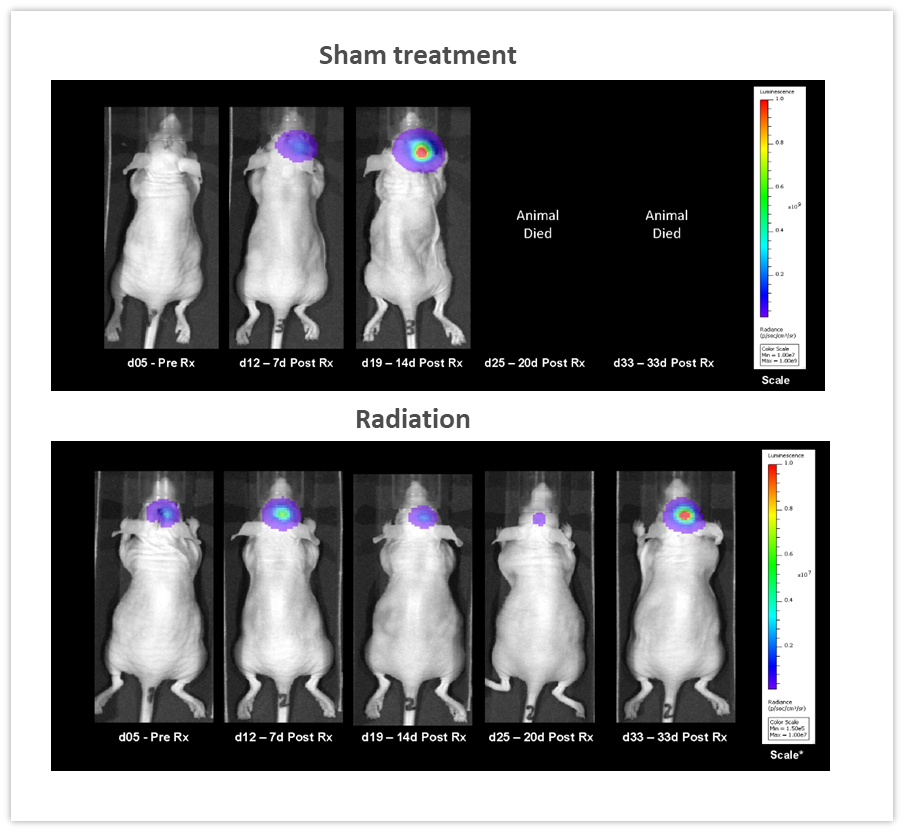
Figure 5 : effet d'une radiothérapie localisée (2 Gy ; 5 jours de traitement, deux jours de repos sur deux cycles) contre le carcinome pulmonaire non à petites cellules NCI-H1975-luc humain implanté par voie intracrânienne chez des souris nude femelles.
Inhibition des points de contrôle et thérapie combinée
L'effet de l'inhibition des points de contrôle, seule ou en combinaison avec des rayons, a été testé sur des cellules de gliome syngénique murin GL261-luc2 implantées par voie intracrânienne chez des souris albinos femelles C57BL/6. Des souris n'ont pas reçu de traitement, ont été traitées par radiations, délivrées par la plate-forme de recherche sur les radiations sur les petits animaux (SARRP ; Xstrahl Inc.), à une dose unique de 7,5 Gy, anti-mPD-1 (clone RMP1-14, 10 mg/kg) ou la combinaison des deux thérapies. Comme le montre la figure 6 (à gauche), le signal BLI était déjà détectable 6 jours après l'implantation des cellules tumorales et a progressé au cours des semaines suivantes. La quantification du signal bioluminescent résultant (à droite) a montré l'effet des traitements sur la charge tumorale. Le traitement anti-mPD-1 a entraîné un retard de croissance de la tumeur de 2,6 jours et 1/8 survivant sans tumeur tandis que les radiations ont entraîné un retard de croissance de la tumeur de 16,6 jours et 2/8 survivants sans tumeur. La combinaison du rayonnement et du traitement anti-mPD-1 a entraîné un retard significatif de la croissance de la tumeur de 38,6 jours et une rémission complète chez les 7/8 souris. Les méthodes traditionnelles de mesure de la réponse anti-tumorale dans les tumeurs enfouies dans le corps sont basées sur des lectures terminales et souvent longues. Comme le montrent ces exemples, l'intégration de l'imagerie BLI in vivo nous a permis de passer d'une thérapie tumorale en « boîte noire » à l'évaluation en temps réel des réponses individuelles, offrant la souplesse nécessaire pour ajuster et affiner les traitements plus rapidement.
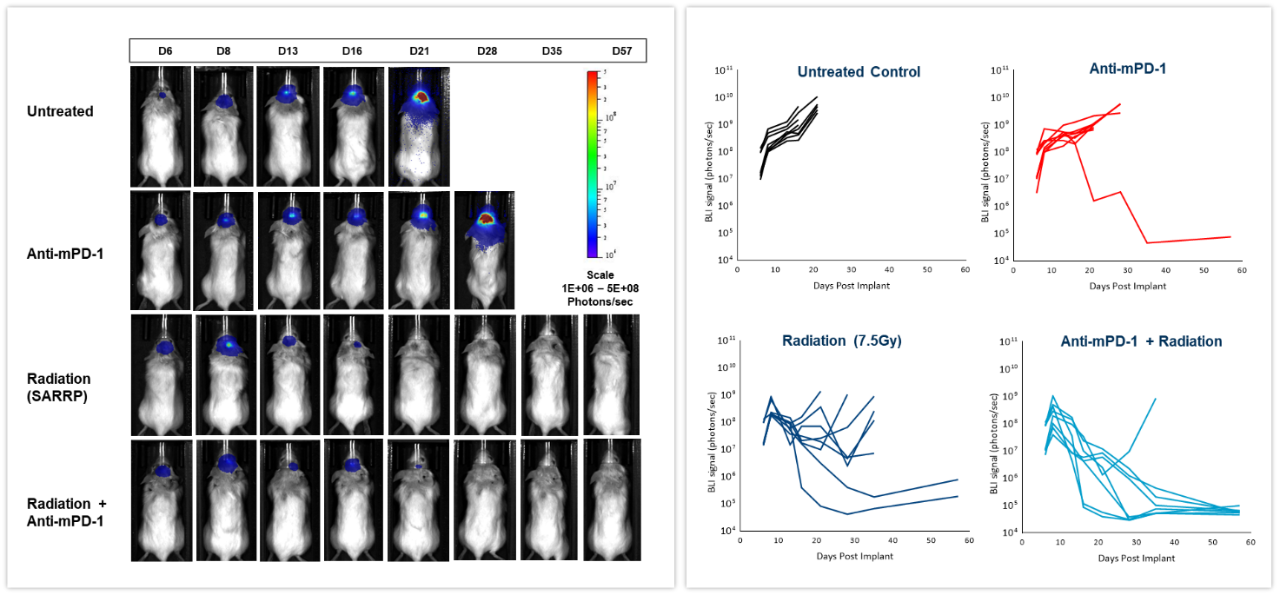
Figure 6 : effet de l'irradiation focalisée, de l'anti-mPD-1 et de la thérapie combinée dans les tumeurs intracrâniennes du GL261-luc chez les souris albinos C57BL/6 femelles.
Multimodalité
La BLI peut être associée à d'autres modalités d'imagerie pour interroger différentes voies biologiques. Pour illustrer cette application, nous avons utilisé des cellules syngéniques 4T1-luc2-1A4 d'adénocarcinome mammaire de souris injectés par OT dans le coussinet adipeux mammaire de souris BALB/c immunologiquement compétentes. Lorsque les tumeurs ont atteint ~300 mm3, un agent d'imagerie dans le proche infrarouge, ProSenseTM750 a été injecté par voie intraveineuse pour détecter l'activité de la cathepsine associée à la croissance agressive du cancer du sein. ProSenseTM750 est un agent optiquement silencieux qui devient fluorescent lors du clivage avec les cathepsines. Comme illustré à la figure 7, les signaux des tumeurs par BLI et FLI étaient facilement détectables dans les tumeurs. Cependant, les signaux BLI et FLI n'étaient pas parfaitement superposables, ce qui est normal étant donné que la luciférase est produite par toutes les cellules tumorales vivantes alors que le signal fluorescent est limité non seulement aux cellules tumorales mais aussi à d'autres cellules associées aux tumeurs, principalement les macrophages, responsables du clivage et de l'absorption de la sonde de cathepsine ProSenseTM750. Multimodality can thus be used to interrogate different biologies in vivo, simultaneously.
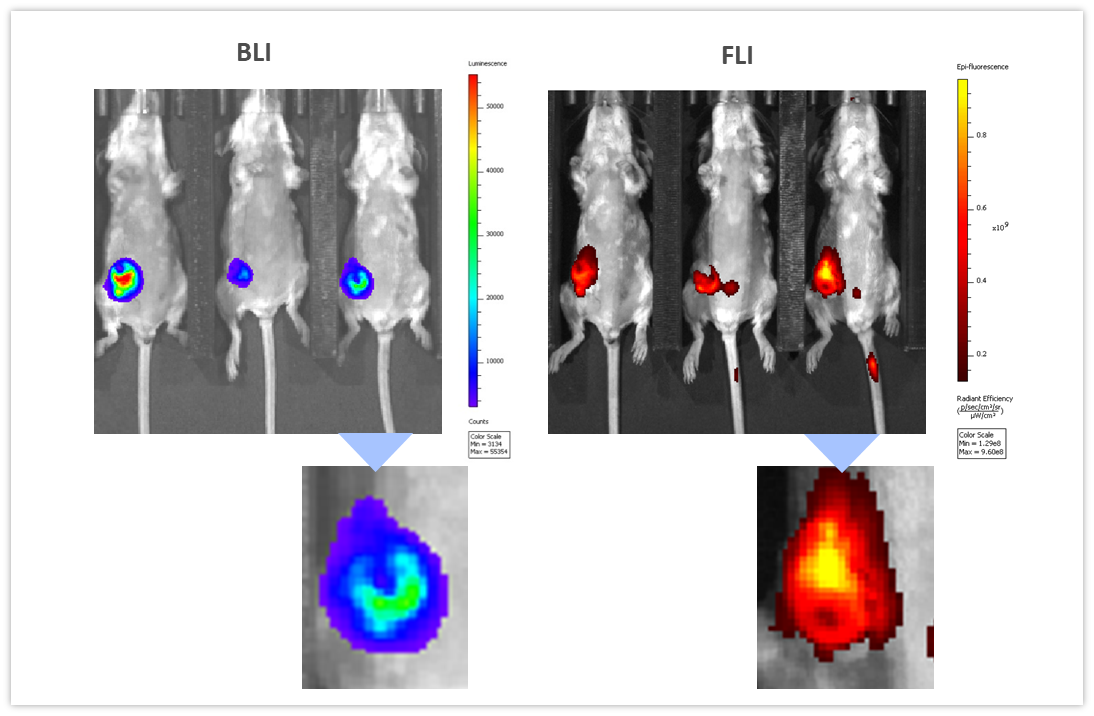
Figure 7 : imagerie multimodale de tumeurs 4T1-luc2-1A4 par BLI (gauche) et FLI (droite) 24 h après injection par voie intraveineuse de la sonde à fluorescence ProSenseTM750 spécifique à la cathepsine. Voyez ci-dessous des gros plans des tumeurs correspondantes.
Résumé
Les modèles murins de cancer des tissus profonds et de métastases cancéreuses reposent principalement sur des évaluations terminales comme le poids des tissus, le nombre de nodules et/ou l'analyse histologique pour l'évaluation de la charge tumorale. Depuis son introduction il y a plus de 20 ans, la BLI est devenue une technique précieuse pour suivre la dynamique de croissance des lignées de cellules cancéreuses marquées par bioluminescence au fil du temps et en réponse à diverses approches thérapeutiques in vivo. Elle permet de réduire au minimum le nombre d'animaux étudiés puisque les images peuvent être extraites des mêmes sujets au fil du temps sans qu'il soit nécessaire de procéder à des évaluations finales. La BLI est à l'origine de contributions importantes dans divers domaines scientifiques, en plus de fournir une alternative à l'utilisation de modalités d'imagerie non invasives établies, invasives ou dépendantes des radio-isotopes.
Contact the scientists to request the full data set or to learn more about our BLI service and how it can be applied to your preclinical research.
Références
1Contag C.H., Spilman S.D., Contag P.R., Oshiro M., Eames B., Dennery P., Stevenson D.K., Benaron D.A. Visualizing gene expression in living mammals using a bioluminescent reporter. Photochem Photobiol 1997; 66: 523–531.
2de Wet J.R., Wood K.V., Helinski D.R., DeLuca M. Cloning of firefly luciferase cDNA and the expression of active luciferase in Escherichia coli. Proc. Natl. Acad. Sci. U.S.A. 1985; 82, 7870–7873.
3 Jenkins D.E., Oei Y., Hornig Y.S., Yu S.F., Dusich J., Purchio T., Contag P.R. Bioluminescent imaging (BLI) to improve and refine traditional murine models of tumor growth and metastasis. Clin Exp Metastasis, 2003; 20(8):733-744.
4 https://www.cancerresearch.org/immunotherapy/treatment-types/adoptive-cell-therapy
Connexion
Entamons le dialogue
Nous contacter