Date: April 2018
In our November 2017 model spotlight, we described the development of a novel syngeneic mouse model of orthotopic ovarian cancer, ID8-Luc. Ovarian cancer remains a significant unmet medical need with a relative 5-year survival rate of 17 % in patients diagnosed with highly advanced stage IV ovarian cancer. Le cancer de l'ovaire est souvent réactif au départ à la chimiothérapie à base de platine et de taxanes, mais les rechutes sont fréquentes.
Nous avons déjà fait état d'une survie médiane de 35 à 40 jours dans le modèle orthotopique ID8 qui s'accompagne du développement d'une ascite péritonéale. Une étude plus approfondie de la progression de la maladie dans les tissus solides à l'aide de l'imagerie par bioluminescence (BLI) ex vivo chez des animaux atteints d'une maladie avancée a permis de détecter la charge de morbidité la plus élevée dans le pancréas, la rate, les ovaires et les cornes utérines.
Tests des inhibiteurs de points de contrôle utilisant les anti-mPD-1 Ab, anti-mPD-L1 Ab et anti-mCTLA-4 Ab
Les modèles de souris syngéniques ont une valeur non négligeable dans la recherche en immuno-oncologie car les souris ont un système immunitaire intact qui permet la manipulation thérapeutique du système immunitaire afin de susciter des réponses antitumorales. En raison de leur avantage clinique dans le mélanome humain et le cancer du poumon non à petites cellules, les inhibiteurs des points de contrôle des cellules T, y compris les anti-PD-1, font l'objet de recherches actives dans les essais cliniques sur le cancer de l'ovaire humain. Pour déterminer si le modèle ID8-Luc de cancer de l'ovaire répondait à l'inhibition du point de contrôle immunitaire, nous avons testé des anticorps anti-mPD-1 Ab, anti-mPD-L1 Ab et anti-mCTLA-4 Ab chez des souris dont la charge tumorale péritonéale ID8 est établie ; en ayant recours à la BLI pour surveiller la réponse thérapeutique (figure 1A). Une forte régression tumorale a été observée chez les souris traitées à la fois avec des anti-MPD-1 (taux de survie sans tumeur de 100 %) ou des anti-MPD-L1 (taux de survie sans tumeur de 100 %) (figure 1B). En revanche, l'anti-mCTLA-4 n'a montré aucune activité significative supérieure à celle d'un anticorps de contrôle d'isotype du rat. Des images représentatives par BLI montrent une charge de morbidité importante chez les souris contrôlées et traitées par des anti-mCTLA-4, alors que les anti-mPD-1 et les anti-mPD-L1 ne présentent aucune maladie détectable (figure 2). L'absence de maladie mesurable a également été confirmée par une autopsie macroscopique à la fin de l'étude.
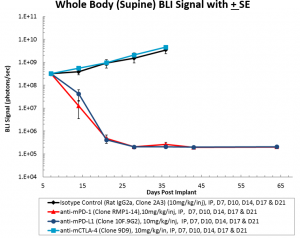
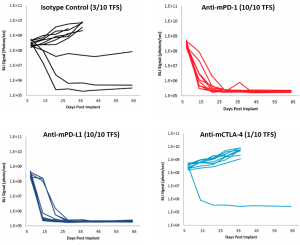
Fig 1 : ID8-luc intrapéritonéale : signal BLI moyen dans le corps entier au fil du temps
Fig 1 : ID8-luc intrapéritonéale : signal BLI individuel dans le corps entier au fil du temps
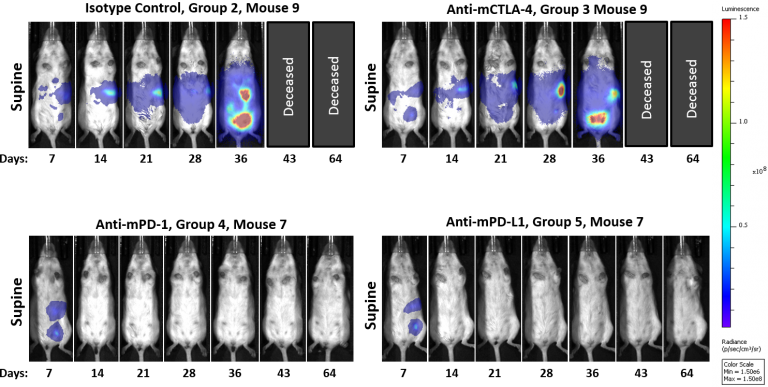
Fig 2 : ID8-luc intrapéritonéale : images représentatives par BLI au fil du temps
Changements de masse corporelle avec inhibiteurs du verrou immunitaire
Le traitement par inhibiteurs de point de contrôle n'a pas été associé à des changements significatifs du poids par rapport aux animaux témoins (figure 3A). La survie médiane des animaux traités par l'anti-mCTLA-4 était comparable à celle des animaux témoins (figure 3B) ; tandis que les souris traitées par l'anti-mPD-1 et l'anti-mPD-L1 représentaient 100 % de survie dans cette étude.
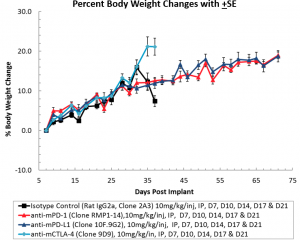
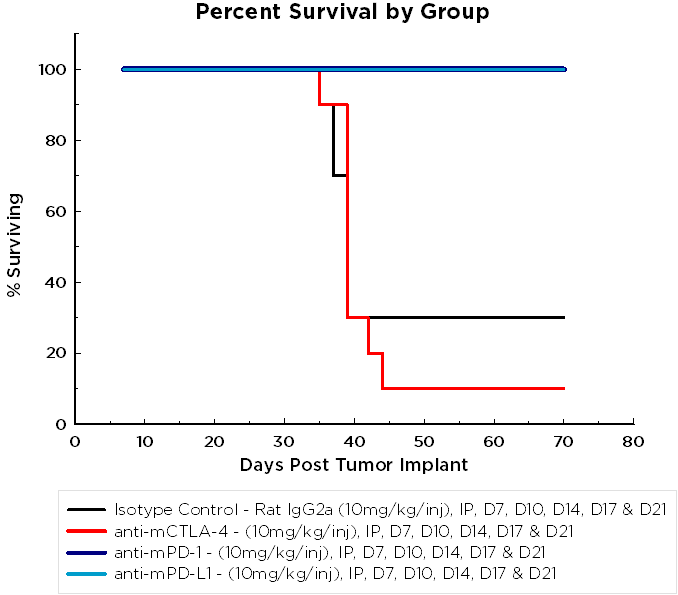
Fig 3 : ID8-luc intrapéritonéale : chagement moyen de la masse corporelle au fil du temps
Fig 3B: ID8 Percent Survival by Group Chart
Évaluation continue des thérapies anti-MPD-1 et anti-MPD-L1
Les souris randomisées pour le début du traitement le 7e jour suivant l'implantation ont un taux de régression spontanée de 10 à 20 % (figure 1B). Pour réduire l'incidence de la régression spontanée et déterminer si la thérapie anti-MPD-1 et anti-MPD-L1 sera aussi efficace avec une charge tumorale plus avancée, nous évaluons actuellement l'activité de ces inhibiteurs de point de contrôle sur des animaux randomisés et traités 14 jours après l'implantation. Nous pensons que ces études fourniront des données permettant des combinaisons rationnelles avec les molécules clients.
Contact Labcorp to speak with one of our scientists to see how ID8 or one of our other syngeneic models can be used for your next immuno-oncology study.
Références
Connexion
Entamons le dialogue
Nous contacter