Date: September 2017
Plus de 90 % de l'ensemble des cancers du pancréas sont classés comme des adénocarcinomes canalaires et, en Occident, le cancer du pancréas est la quatrième cause de décès liés au cancer.
Le pronostic du cancer du pancréas est extrêmement dévaforable avec un taux de survie relative à 5 ans de 5 % et une survie médiane de 3,5 mois pour les patients atteints de tumeurs non résécables de stade III 1. Malheureusement, l'incidence du cancer du pancréas a augmenté alors que le taux de survie à 5 ans n'a pas changé. La résection chirurgicale est la seule thérapie potentiellement curative, mais seulement 10 % des patients sont diagnostiqués assez tôt pour qu'elle soit envisageable et la plupart de ceux qui sont admissibles à la chirurgie finissent par rechuter. Comme beaucoup d'autres types de cancer, le cancer du pancréas se développe silencieusement pendant des années, sans aucun symptôme. Dans la plupart des cas, le diagnostic n'est posé que lorsque le cancer s'est développé en dehors du pancréas vers d'autres tissus proches et/ou s'est métastasé. Ces patients n'ont que très peu d'options valables. C'est pourquoi de nouvelles thérapies efficaces font cruellement défaut dans le traitement du cancer du pancréas.
Depuis 15 ans, les patients diagnostiqués avec un cancer du pancréas à un stade avancé reçoivent de la gemcitabine (Gemzar®) comme traitement standard de première ligne. En phase préclinique, nous utilisons la gemcitabine comme standard de soins afin de fournir une référence à nos clients qui cherchent à faire mieux que les options de traitement clinique actuelles ou à les combiner avec de nouvelles thérapies, telles que des agents ciblés et des immunomodulateurs.
Il existe plusieurs lignées de cellules pancréatiques humaines et murines à la disposition des chercheurs en oncologie en phase préclinique pour favoriser le développement de nouvelles thérapies. Labcorp has a large panel of pancreatic lines ready for testing (see Table 1). Nous avons optimisé et caractérisé la croissance sous-cutanée (SC) pour plusieurs de ces modèles et évalué leur réponse au traitement à la gemcitabine.
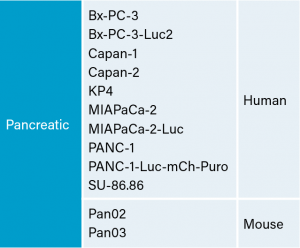
Table 1: Pancreatic Carcinoma Cell Lines at Labcorp
PANC-1
PANC-1 a été isolé chez un homme caucasien de 56 ans atteint d'un adénocarcinome canalaire pancréatique. La croissance tumorale sous-cutanée est fiable et régulière, le volume de la tumeur doublant tous les 5 jours et atteignant généralement la taille d'évaluation (~750 mm3) environ 29 jours après l'implantation. Le traitement à la gemcitabine (160 mg/kg) est bien toléré et produit un retard de croissance tumorale statistiquement significatif, mais il n'est pas curatif (voir les figures 1 et 2).
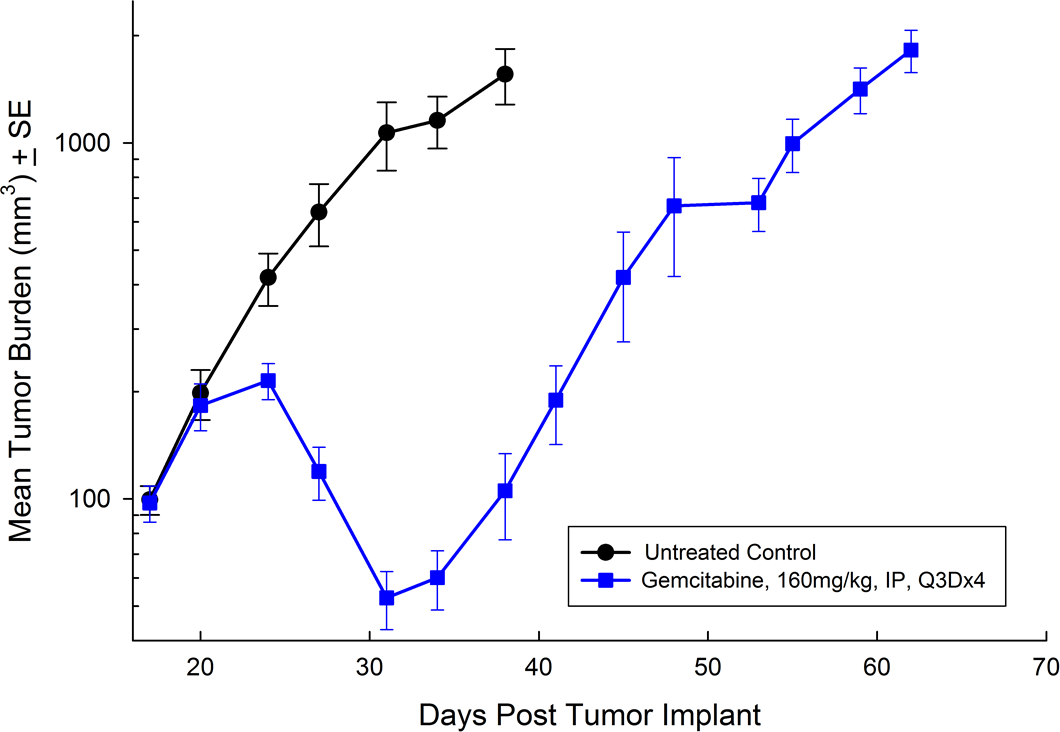
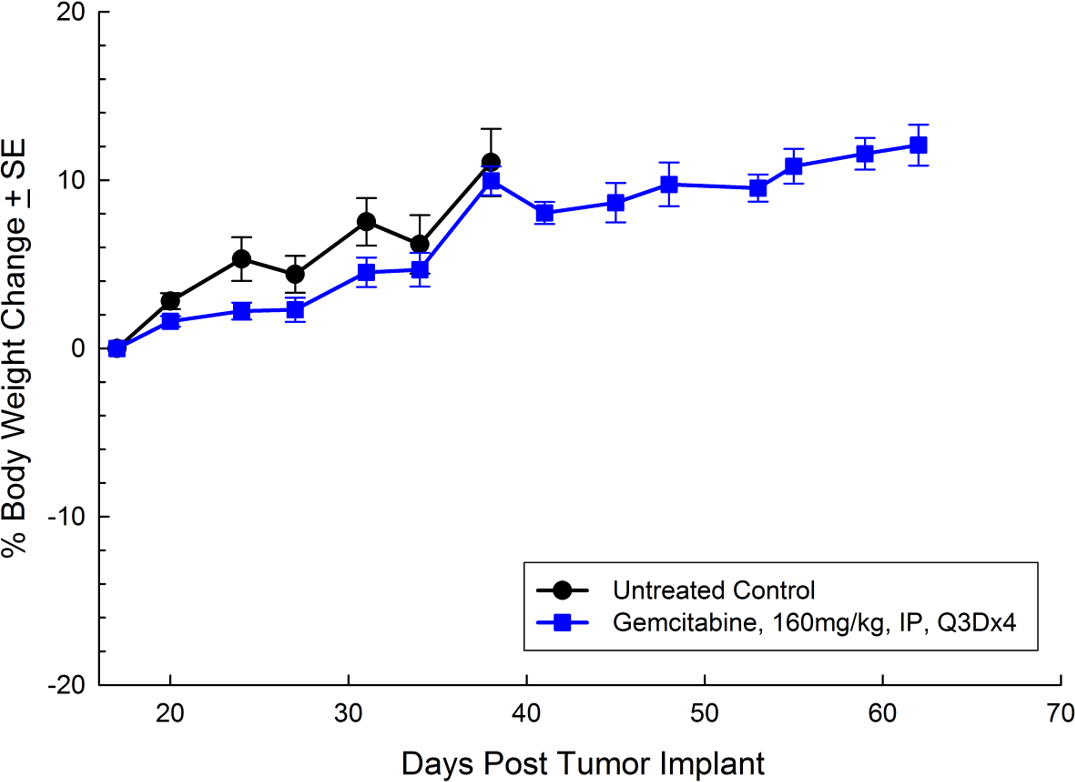
Fig. 1 : charge tumorale moyenne de PANC-1 en sous-cutané avec erreur type
Fig. 2 : évolution du poids corporel en pourcentage avec PANC-1 en sous-cutané avec erreur type
Capan-2
Capan-2, isolé chez un homme caucasien de 56 ans atteint d'un adénocarcinome canalaire pancréatique, présente une croissance tumorale sous-cutanée un peu plus lente que PANC-1 avec un doublement du volume de la tumeur en environ 12 jours et un temps nécessaire pour atteindre la taille d'évaluation (750 mm3) d'environ 36 jours après l'implantation. Le traitement à la gemcitabine (112 mg/kg) est bien toléré et produit un retard de croissance tumorale statistiquement significatif, avec un grand nombre de survivants sans tumeur (voir les figures 3 et 4).
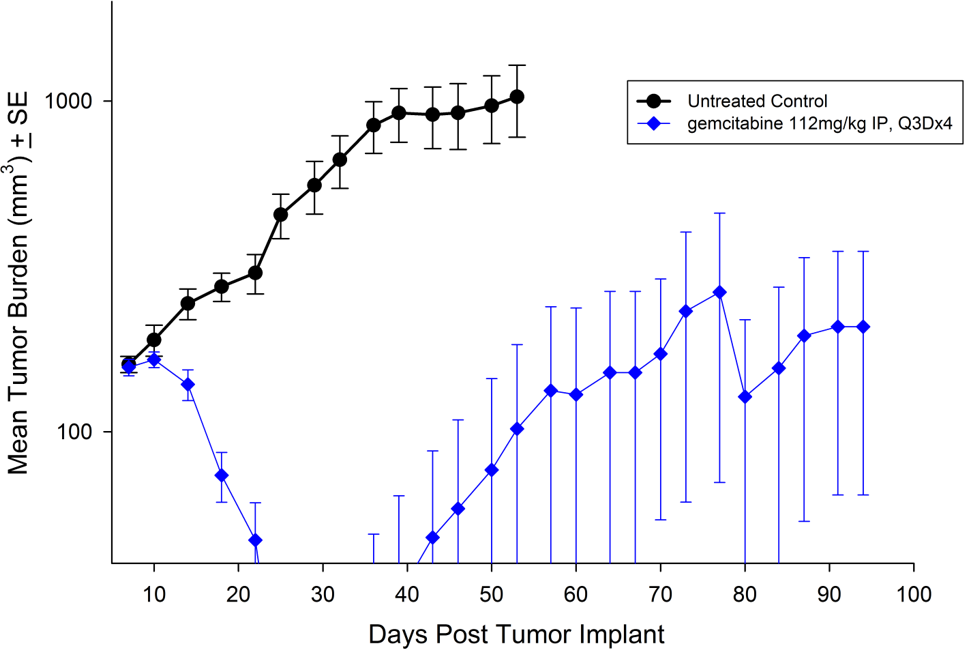
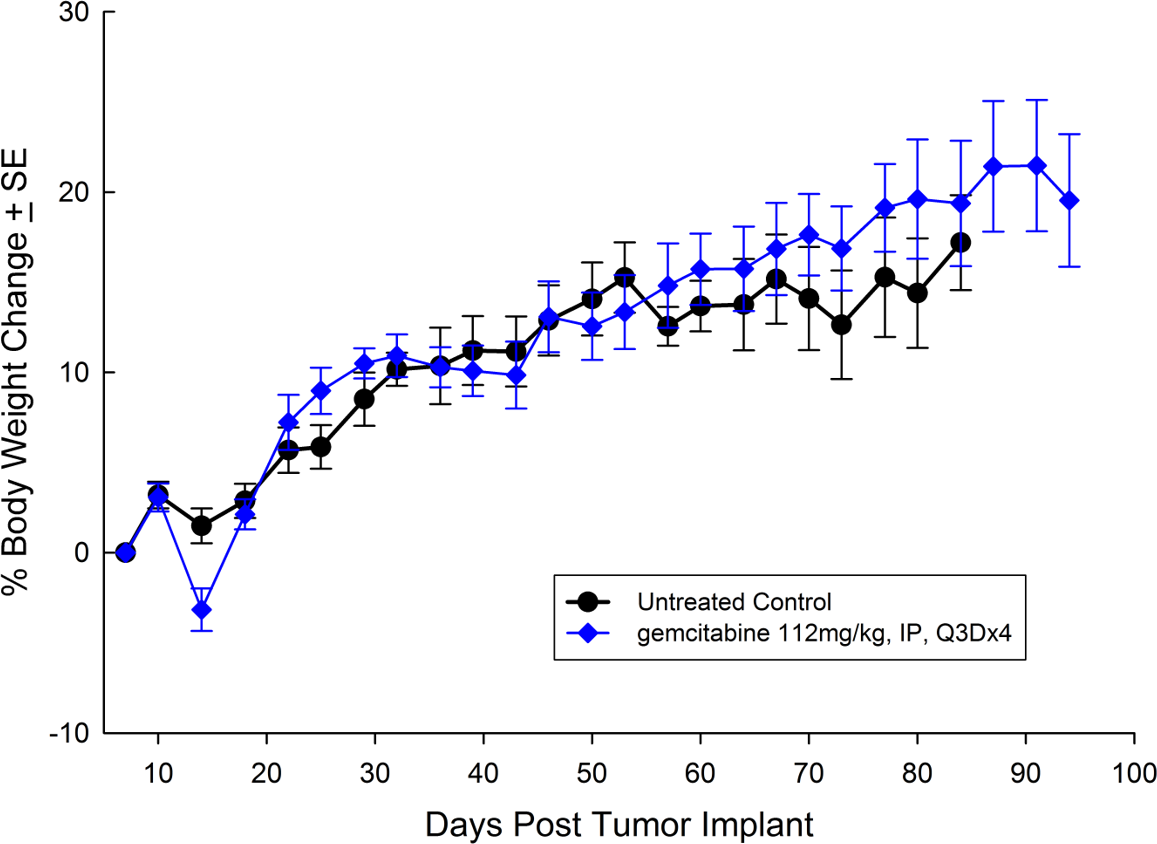
Fig. 3 : charge tumorale moyenne de Capan-3 en sous-cutané avec erreur type
Fig. 4: Subcutaneous Capan-2 % Body Weight Change with Standard ErrorCapan-2
Bx-PC-3
Bx-PC-3 a été isolé chez une femme caucasienne de 61 ans atteinte d'un adénocarcinome pancréatique. La croissance sous-cutanée de la tumeur entraîne un doublement du volume de la tumeur en environ 16 jours et le temps nécessaire pour atteindre la taille d'évaluation (750 mm3) est d'environ 38 jours après l'implantation. Le traitement à la gemcitabine (80 mg/kg) est bien toléré mais ne produit pas de retard de croissance tumorale statistiquement significatif (voir les figures 5 et 6).
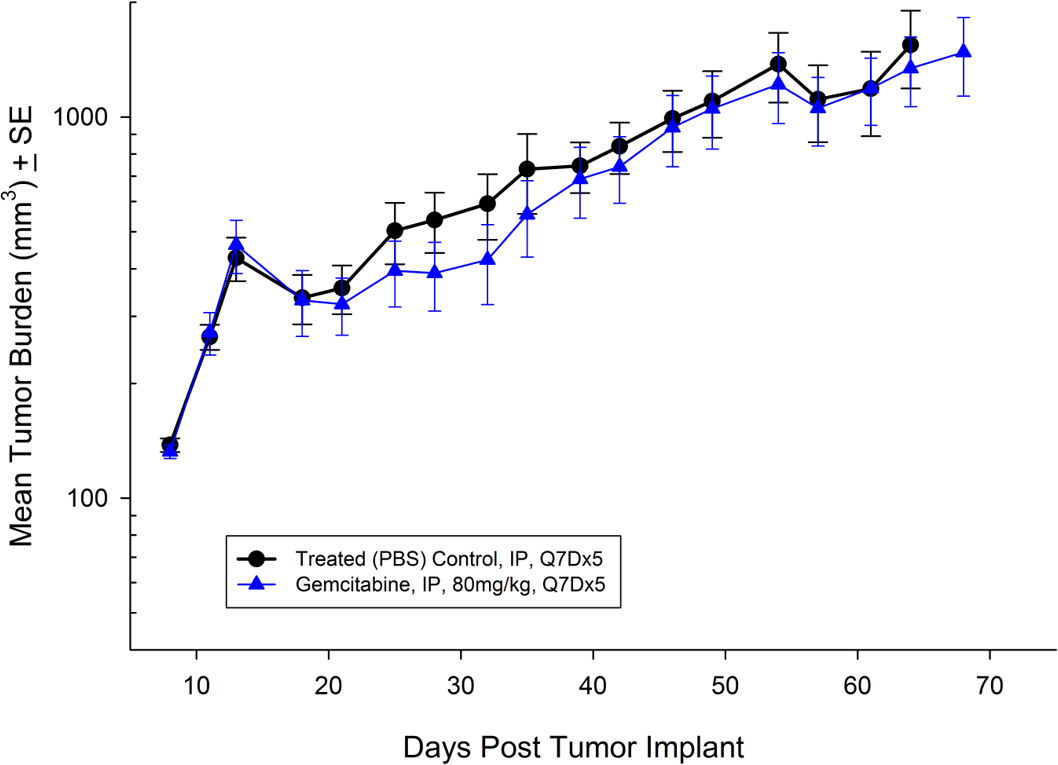
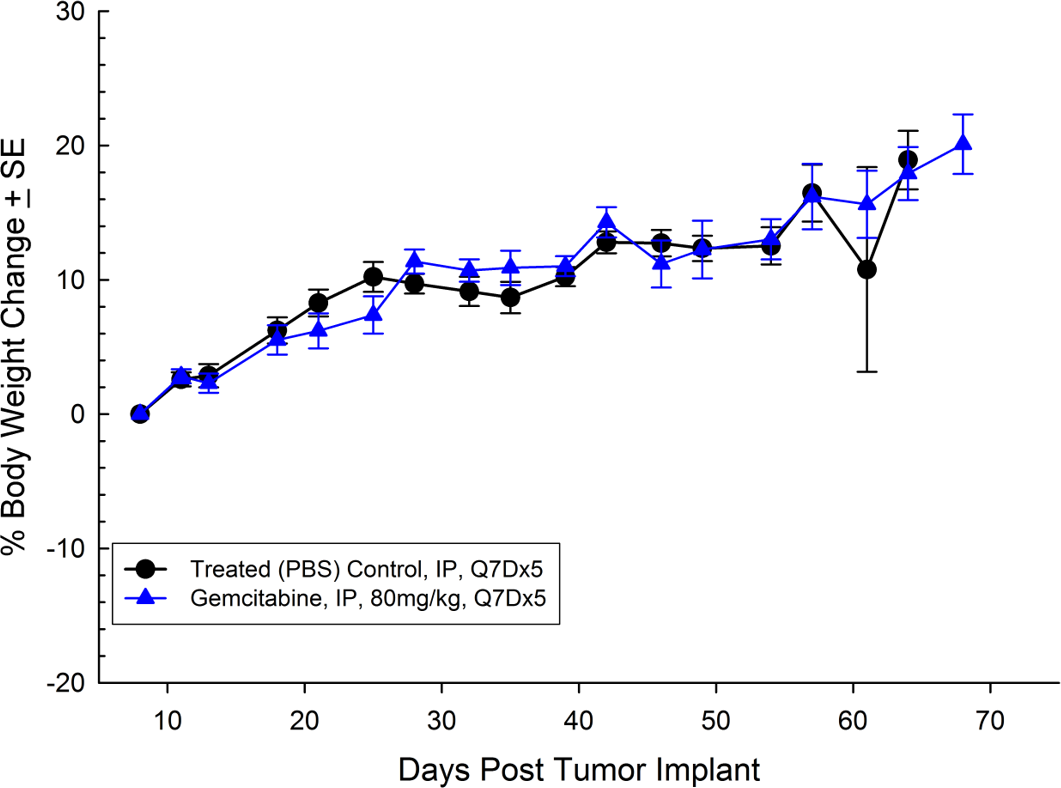
Fig. 5 : charge tumorale moyenne de Bx-PC-3 en sous-cutané avec erreur type
Fig. 6 : évolution du poids corporel en pourcentage avec Bx-PC-3 en sous-cutané avec erreur type
MIAPaCa-2
MIAPaCa-2 a été isolé chez un homme caucasien de 65 ans atteint d'un carcinome pancréatique. Ce modèle montre une croissance tumorale sous-cutanée très agressive avec un temps de doublement du volume de la tumeur d'environ 3 jours et un temps nécessaire pour atteindre la taille d'évaluation (750 mm3) d'environ 21 jours après l'implantation. Le traitement à la gemcitabine (160 mg/kg) est bien toléré et produit un retard de croissance tumorale statistiquement significatif, avec un survivant sans tumeur observé dans l'étude (voir les figures 7 et 8).
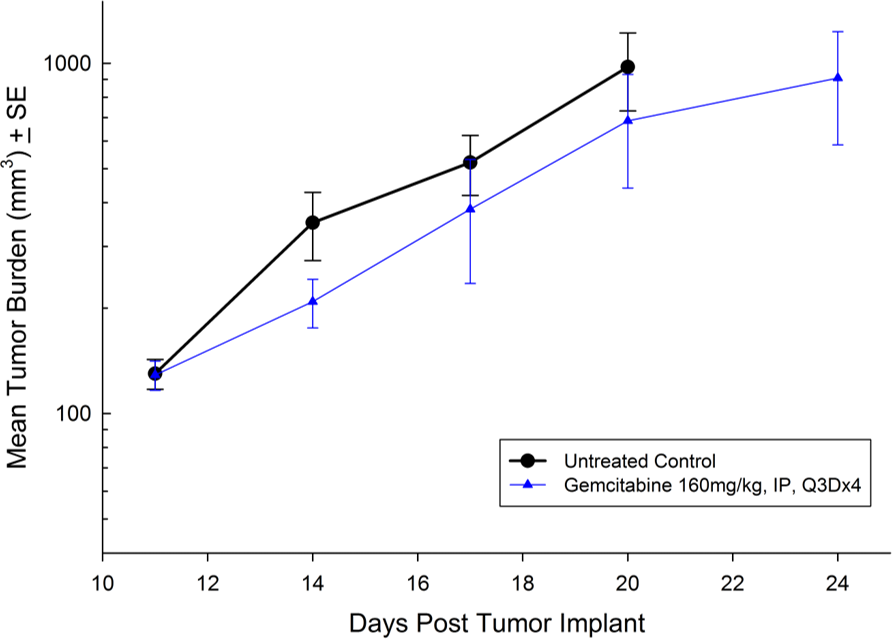
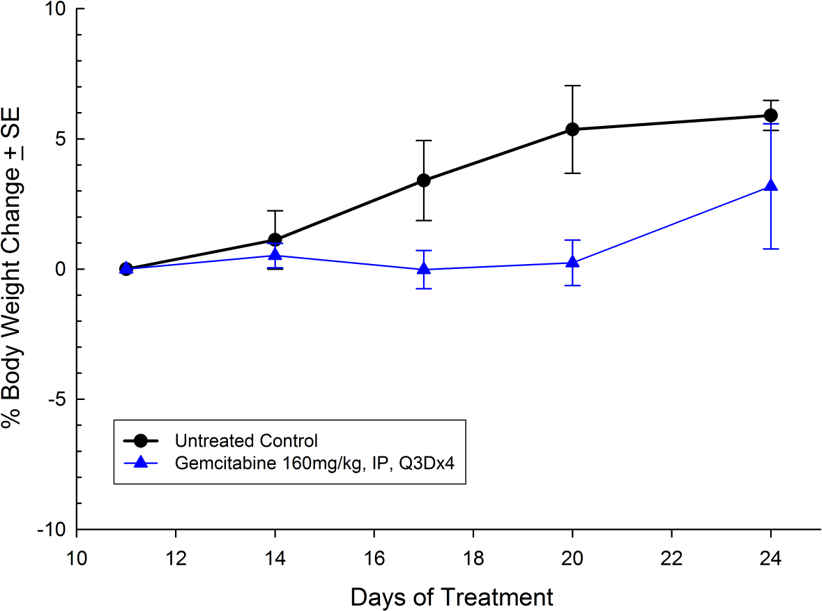
Fig. 7 : charge tumorale moyenne de MIAPaCa-2 en sous-cutané avec erreur type
Fig. 8 : évolution du poids corporel en pourcentage avec MIAPaCa-2 en sous-cutané avec erreur type
Comme pour la réponse clinique aux normes de soins, la réponse au traitement préclinique dépend fortement de la lignée tumorale utilisée. De nombreux facteurs peuvent contribuer à la réactivité ou à l'absence de réactivité au traitement à la gemcitabine. Cependant, l'examen de plusieurs lignes de tumeurs différentes dans une même indication peut fournir des informations clés sur l'efficacité d'une nouvelle thérapie dans la phase clinique.
Please contact us if you are interested in discussing any of our pancreatic models.
Références
Connexion
Entamons le dialogue
Nous contacter