Auteur : Maryland Franklin, PhD, vice-présidente du développement scientifique
Date: June 2017
Alors que la contribution directe du CD19 aux cancers des lymphocytes B humains est toujours à l'étude, son expression se retrouve sur une majorité de tumeurs malignes des lymphocytes B. Par exemple, la leucémie aiguë lymphoblastique (LAL), les lymphomes à lymphocytes B et les leucémies à lymphocytes B présentent respectivement une expression de 80 %, 88 % et 100 % de CD19. 1 La LAL se caractérise par une surproduction de lymphoblastes dans la moelle osseuse qui se multiplient continuellement, entraînant l'inhibition de la production normale de cellules hématopoïétiques.
La LAL est plus fréquente chez les jeunes enfants, mais elle se manifeste également chez les adultes. Les enfants ont un taux de guérison supérieur à 80 %, alors que chez les adultes le taux de guérison est de 20-30 % seulement. Une maladie similaire est la leucémie lymphocytaire chronique (LLC) qui est généralement diagnostiquée chez les personnes âgées. La LLA et la LLC ont toutes deux été identifiées comme des affections malignes pouvant faire l'objet de thérapies dirigées contre le CD19. Alors que les anticorps monoclonaux anti-CD19 et d'autres approches sont étudiées pour le développement clinique, l'approche de loin la plus courante pour cibler les malignités liées au CD19 est celle des cellules T modifiées par le récepteur d'antigène chimérique (CAR-T). Le CD19 a été la première cible utilisée pour cette stratégie de thérapie par cellules T et reste un domaine d'investigation clinique actif.
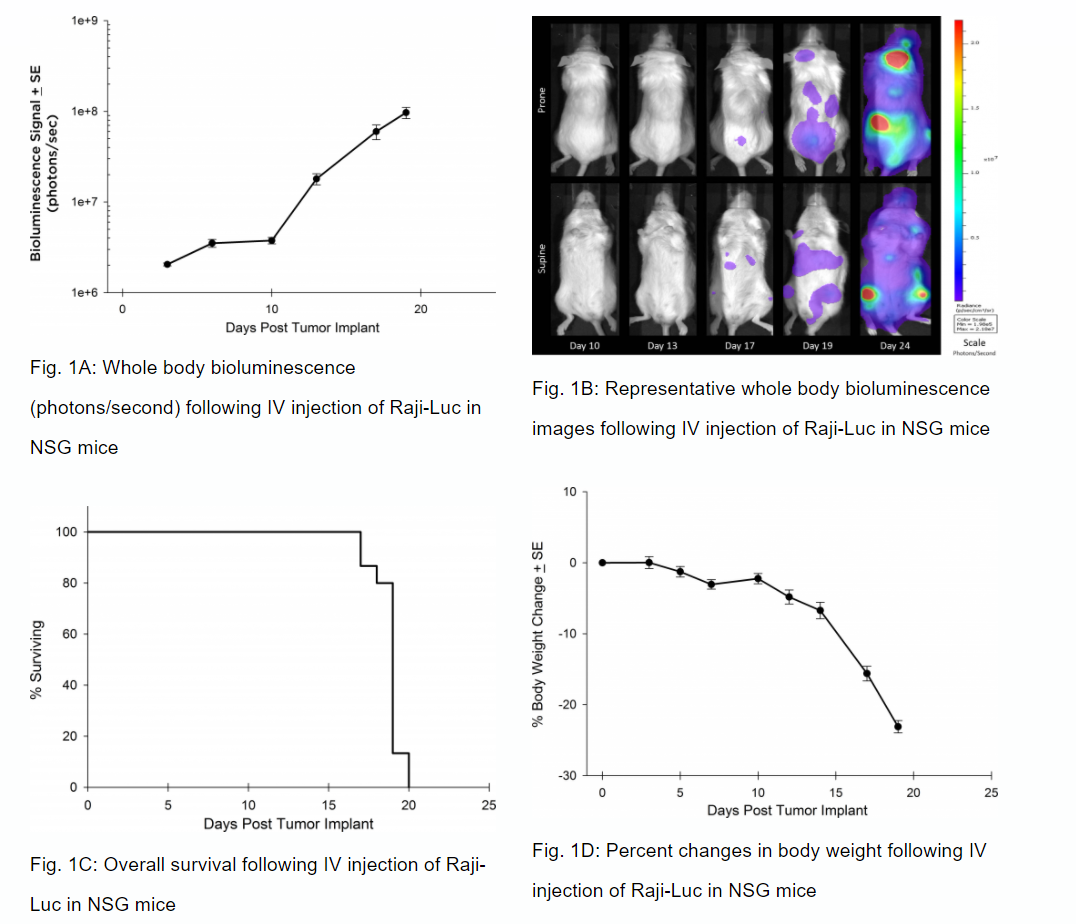
Sur le plan préclinique, la lignée de cellules de lymphome humain de Burkitt, Raji, a été un élément essentiel pour déterminer l'activité anti-tumorale des approches liées aux malignités des cellules B. At Labcorp, we employ a luciferase-expressing Raji cell line (Raji-Luc) to allow us to track disease progression and therapeutic response over time through in vivo optical imaging. Raji-Luc est un excellent modèle pour évaluer les thérapies CAR-T dirigées contre le CD19. Nous avons utilisé ce modèle chez la souris SCID et NSG pour plus d'une douzaine d'études sur les CAR-T ou d'autres thérapies cellulaires. Dans de nombreux cas, la souche de souris la plus immunodéficiente, la souris NSG, est nécessaire à la survie et à la persistance de la thérapie cellulaire. Ainsi, nous avons validé la croissance du modèle Raji-Luc chez la souris NSG grâce à l'imagerie par bioluminescence (BLI) in vivo (figures 1A & B) et constaté une diffusion agressive de la maladie comme l'illustre le critère de survie globale d'environ 20 jours (morbidité/mortalité, figure 1C). Conformément à l'induction rapide de la maladie, les souris ont présenté une perte de poids corporel progressive (figure 1D) et une paralysie complète des membres postérieurs qui a nécessité l'euthanasie.
Validation de la croissance de Raji-Luc chez la souris NSG
Activité anti-tumorale des anticorps monoclonaux anti-CD20 - Rituximab
Tout comme le CD19, le CD20 est également un marqueur des cellules B et a été une cible initiale des médicaments destinés aux malignités des cellules B comme le lymphome non hodgkinien. Le développement clinique de l'anticorps monoclonal anti-CD20, le rituximab, s'est avéré révolutionnaire pour l'utilisation des anticorps monoclonaux comme traitement en oncologie. Chez les souris SCID, nous avons testé l'activité anti-tumorale du rituximab et démontré une augmentation de la survie globale (figure 2A) en corrélation avec une réduction de la charge tumorale du corps entier déterminée grâce à l'imagerie par bioluminescence (BLI)in vivo (figures 2B et 2C). Comme lors des études menées sur des souris NSG, nous avons observé des signes cliniques d'évolution de la maladie comme la paralysie des membres postérieurs et la perte de poids (figure [#0]}D). En plus de la BLI in vivo, nous avons également examiné l'incidence de la maladie dans divers tissus avec la BLI ex vivo (tableau 1). Grâce à des analyses ex vivo, nous avons en outre démontré que le traitement au rituximab réduisait la charge de morbidité globale.
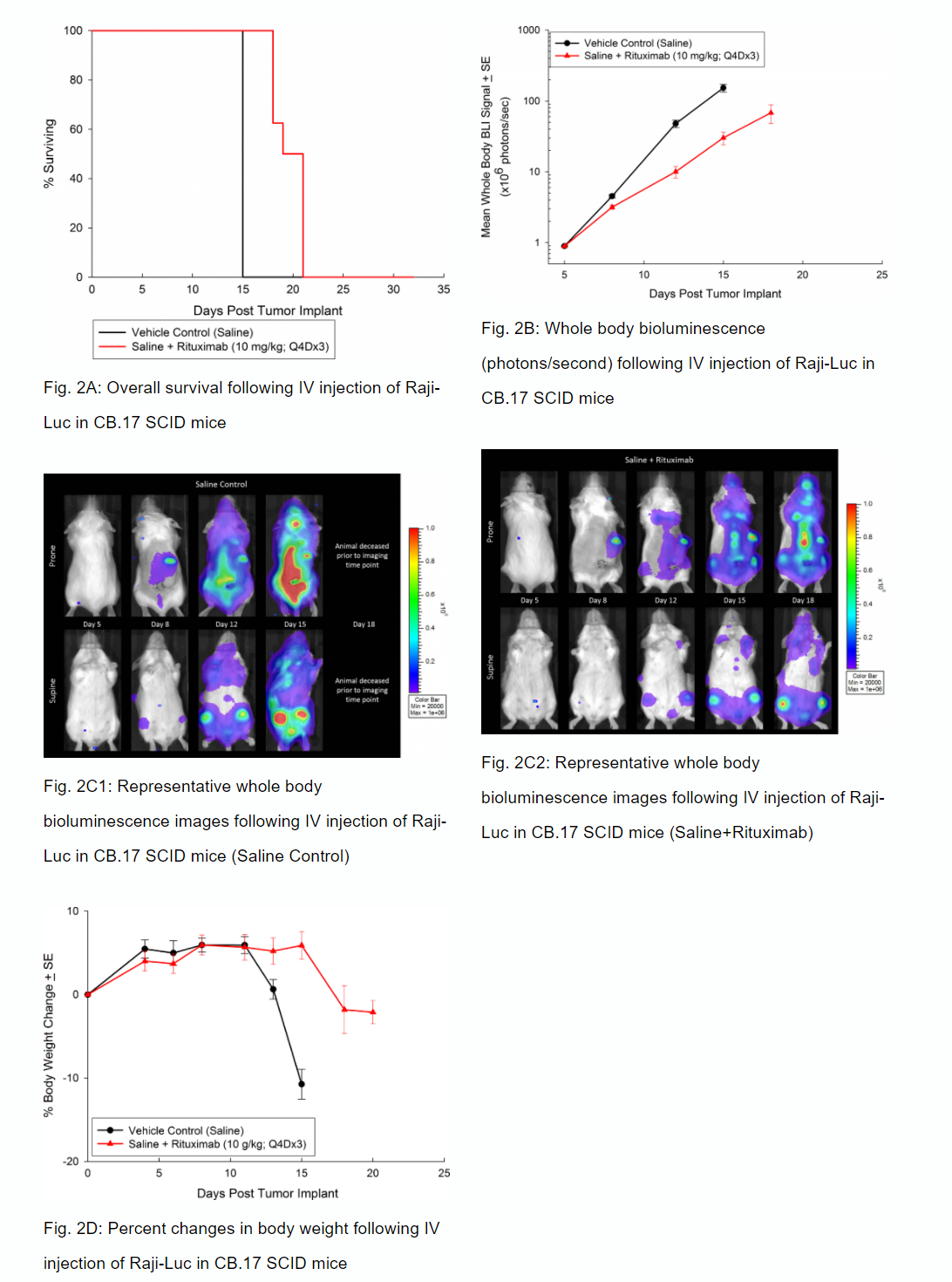
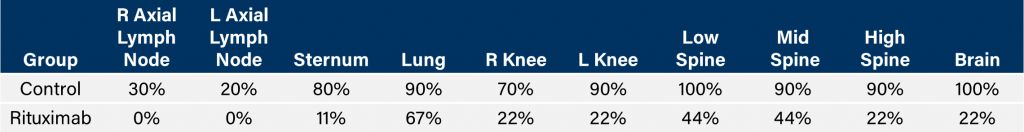
Tableau 1 : incidence de la dissémination de la maladie après injection par voie intraveineuse de Raji-Luc chez la souris CB.17 SCID.
Évaluation du modèle Raji-Luc par voie sous-cutanée chez la souris SCID
Si la plupart des approches thérapeutiques ont utilisé le modèle Raji-Luc après une implantation par voie intraveineuse, dans certains cas, les stratégies anti-tumorales nécessitent une évaluation sous-cutanée (SC). Pour cela, nous avons validé la croissance de la lignée Raji-Luc par voie sous-cutanée sur des souris SCID. La lignée se développe assez rapidement avec un temps de doublement de quatre jours et environ 27 jours entre l'implantation et le moment où les critères pour pratiquer l'euthanasie sont respectés (figure 3).
![Fig. [#0]} : croissance sous-cutanée de cellules Raji-Luc implantées par voie sous-cutanée chez la souris CB.17 SCID](https://biopharma.labcorp.com/industry-solutions/by-therapeutic-area/oncology/preclinical/tumor-spotlights/targeting-b-cell-malignancies-raji-luc-model-test-cd19-directed-car-t-cells-novel-approaches/_jcr_content/root/responsivegrid_left/image_copy_copy_copy.coreimg.png/1670865878260/1577976679053.png)
Fig. [#0]} : croissance sous-cutanée de cellules Raji-Luc implantées par voie sous-cutanée chez la souris CB.17 SCID
Ainsi, Raji-Luc, que ce soit dans le cadre de souris SCID ou NSG, fournit un modèle rapide permettant de tester les thérapies dirigées contre le CD19 ou le CD20.
Contact us to speak with one of our scientists about how Raji-Luc or one of our other models can be used for your next CAR-T study.
Références
Connexion
Entamons le dialogue
Nous contacter